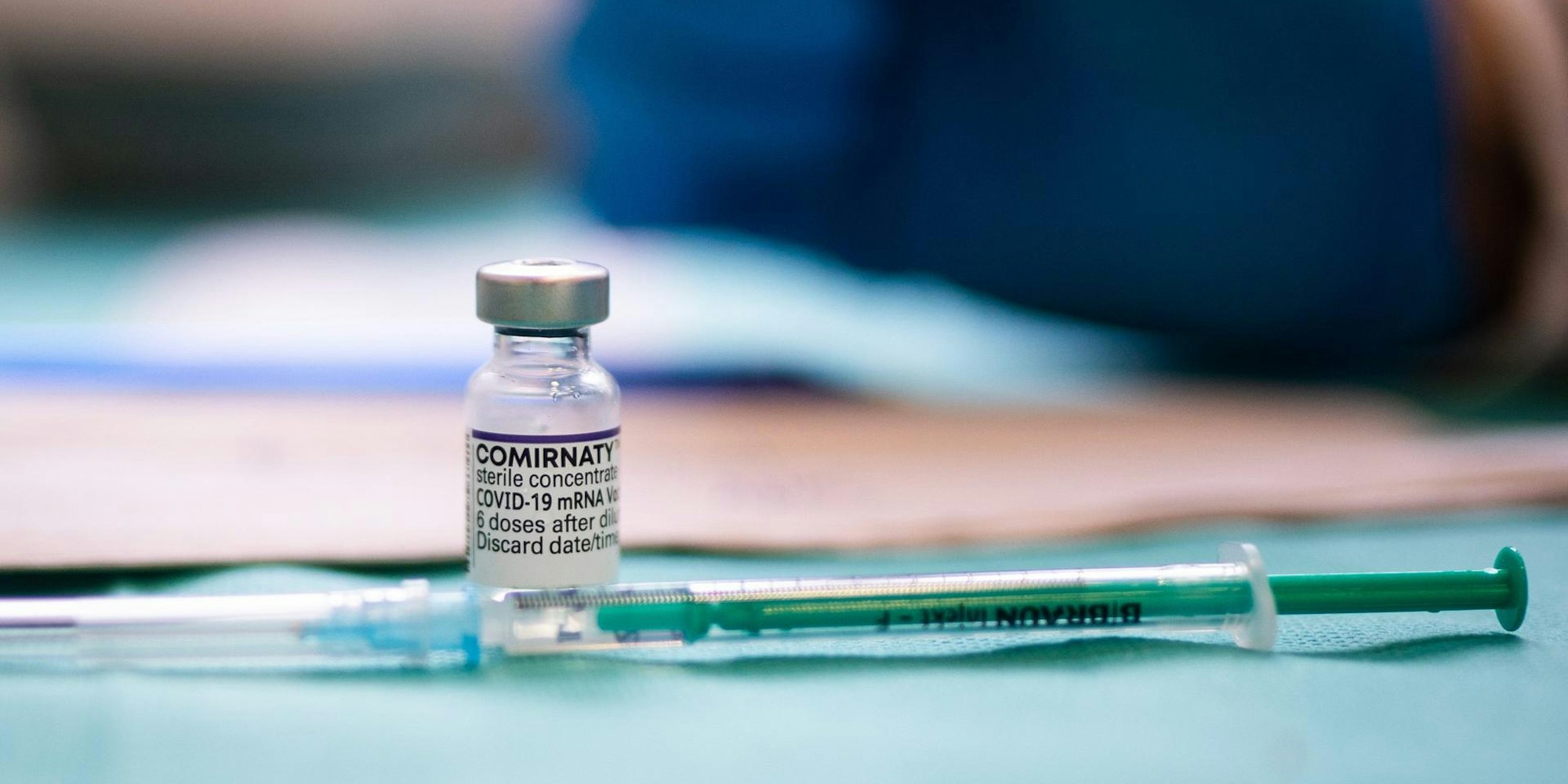
In Deutschland und in vielen anderen Ländern grassiert die Omikron-Variante - vor der bisherige Impfstoffe nur begrenzten Schutz bieten. Als erste Hersteller haben nun Biontech und Moderna angepasste Vakzine angekündigt. Doch bei den Impfstoffen der neuen Generation ist das Wettrennen einiges gemächlicher als noch vor anderthalb Jahren.
Mehrere Impfstoffhersteller hatten schon bei der Entdeckung der Omikron-Variante Ende November angekündigt, eventuell angepasste Vakzine entwickeln zu wollen. Ende vergangener Woche kündigten Biontech und Pfizer gemeinsam an, im März liefern zu können. Moderna will dann die Zulassung beantragen.
Während die Anpassung bei mRNA-Impfstoffen vergleichsweise schnell geht, stellt das Zulassungsverfahren eine größere Hürde dar: Die Europäische Arzneimittelagentur (EMA) visiert diese erst für April oder Mai an, wie vergangene Woche der EMA-Impfstrategie-Chef Marco Cavaleri sagte. „Wir wünschen uns eine schnelle Zulassung“, kritisierte Bundesgesundheitsminister Karl Lauterbach (SPD) prompt gegenüber der Wirtschaftswoche.
EMA lässt sich Zeit
Der Grund für die Verzögerung: Die EMA schon im vergangenen Jahr ein beschleunigtes Zulassungsverfahren für angepasste Impfstoffe auf den Weg gebracht, angewandt wurde es bislang aber nicht. Nun würden Details des Verfahrens konkretisiert, erklärte Rolf Hömke, beim Pharmaverband VFA Sprecher zu Forschungsthemen, gegenüber dem RedaktionsNetzwerk Deutschland.
„Das kann zur Konsequenz haben, dass die Studienergebnisse später vorliegen und bewertet sind, als erste Kontingente an lieferfähigem Impfstoff bereitstehen“, bestätigte Hömke Lauterbachs Sorgen. Die Verspätung sieht er aber gelassen. Die Bevölkerungen brauche die Bestätigung, dass es sich um auf Wirksamkeit und Verträglichkeit geprüfte Produkte handele: „Dafür ist das EMA-Zulassungsverfahren da“.
Bislang ist unklar, ob Anpassungen nötig sind
Und so könnte es sein, dass in Deutschland produzierter Impfstoff im März und April irgendwo auf der Welt verimpft wird, während Europäer noch warten müssen. Aus Sicht der EMA ist das womöglich vertretbar: Cavaleri hatte zuletzt zu den schon verfügbaren Auffrischungsimpfungen geraten und betont, Omikron bringe „offenbar weniger schwere Krankheitsverläufe“ mit sich.
Die Vakzine von Biontech und Moderna bieten -besonders nach einer Auffrischungsimpfung- zwar einen ordentlichen Schutz vor schweren Erkrankungen. Doch so gut wie gegen den Wildtyp und frühere Mutationen des Coronavirus wirken sie nicht, wie mittlerweile zahlreiche Studien belegen. Wie dringend verbesserte Impfstoffe nötig sind, ist allerdings auch bei der Weltgesundheitsorganisation unklar. Eine Empfehlung, Vakzine anzupassen, haben die zuständigen WHO-Gremien bislang nicht ausgesprochen - obgleich sie das Thema ausdrücklich im Blick haben.
Das könnte Sie auch interessieren:
Andere Impfstoffhersteller haben bislang noch keine Updates oder gar neue Impfstoffe angekündigt. Einige preisten zuletzt eine passable Wirkung ihrer Produkte gegen Omikron an. Der Totimpfstoff von Valneva etwa ist zwar nicht auf die neue Variante gemünzt, aber laut Hersteller gegen Omikron zu 87 Prozent wirksam. Valneva hofft auf eine europäische Zulassung im ersten Quartal 2022.
Curevac hält sich weiterhin zurück
Zugleich ermöglicht es vor allem die von Biontech und Moderna genutzte mRNA-Technologie, Vakzine vergleichsweise rasch anzupassen. Der ebenfalls auf mRNA-Technologie setzende Hersteller Curevac plant bislang trotzdem kein Omikron-Update. Derzeit werde noch geprüft, ob ein speziell auf die Omikron-Variante ausgerichteter Impfstoff nötig ist, erklärte eine Sprecherin des Tübinger Unternehmens.
Nachdem ein erster Curevac-Impfstoff am Zulassungsverfahren gescheitert war, arbeitet Curevac schon länger an einem neuen mRNA-Vakzin. Dessen Immunreaktion gegen Omikron werde gerade „mit Hochdruck“ bei Labortests überprüft, sagte die Sprecherin. Parallel würden klinische und produktionstechnische Abläufe darauf ausgerichtet, einen Omikron-spezifischen Impfstoff in die geplanten Studien aufzunehmen - „falls erforderlich“, wie die Sprecherin hinzufügte.
Bei Biontech und Pfizer scheint man sich ebenfalls des Risikos, dass ein Omikron-Impfstoff keinen reißenden Absatz finden könnte, bewusst zu sein. Es sei immer noch nicht klar, ob ein Omikron-Impfstoff benötigt werde, hatte Pfizer-Chef Albert Bourla vergangene Woche gesagt. „Wir haben mit der Produktion auf eigenes Risiko begonnen,“ so der Firmenlenker gegenüber dem US-Fernsehsender CNBC.